アルツハイマー病 (Alzheimier's disease, AD) 等の変性疾患を研究する人達ならほぼほぼお世話になっているであろう、Alzforum。
今年も例年通り、2020年のまとめと、2021年の展望を発表しました。
2020年を振り返って
昨年は、COVID-19の影響で、AD患者さんは、社会的隔離による認知症症状の悪化に苦しみました。
また、研究者達にも大きな影響を与え、毎年 30,000人近くが参加する SfNのカンファレンスも中止となりました。
いくつかの臨床試験は中止となりましたが、他の試験は解析が進められ、アデュカヌマブがFDAの審査を受けるところまできました。
AD治療薬
抗Aβ治療薬
アデュカヌマブ(aducanumab)
アデュカヌマブの話題については、このブログでも何度か取り上げました。
一度は効果が期待できないと中止を余儀なくされましたが、
その後も解析を重ねて「ポジティブな結果が得られた」と主張し、FDA申請を行って私達をおどろかせました。
色々厳しい意見もありますが……どうなるでしょうか。
今年の3月5日までには決定が下る予定です。
バイオジェンとエーザイが、アルツハイマー病による軽度認知障害(MCI due to AD)および軽度AD患者を対象にした、 アデュカヌマブの有効性、安全性を評価する臨床第III相国際共同試験(ENGAGE試験、EMERG …
半年ほど前にPhase 3 trialが失敗に終わった……と思われていたAducanumabですが、 Biogenの自社グループがデータを再検証・再解析した結果、有意にポジティブととらえられたため、FDAの承認を目指して …
昨日、バイオジェンとエーザイがアルツハイマー病 (Alzheimer's disease, AD) 治療薬としてアデュカヌマブの申請を完了したとアナウンスしました。 承認されれば、ADに対する初の疾患修飾療法(desea …
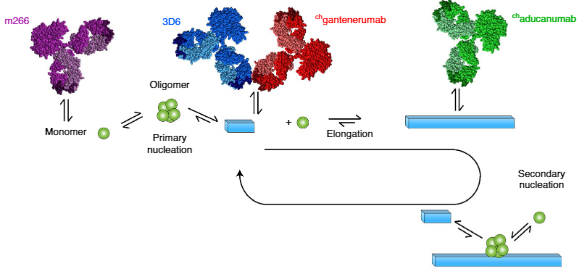
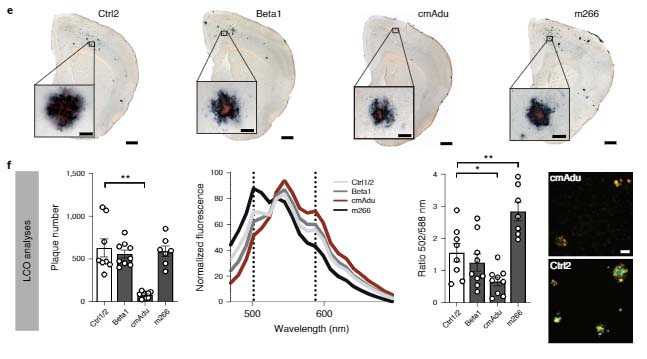
1999年にSchenkらの研究グループがアミロイドβ(Amyloid beta, Aβ)抗体による、ADモデルマウス脳内のAβプラーク消失と認知機能改善を報告 [1] して以来、現在まで多くのAβ抗体が開発され、臨床応 …
先月6日に行われたFDAのアデュカヌマブミーティングではだいぶ旗色が悪く、FDA承認は難しそうな印象ですが、 少なくともマウス脳内では成績優秀のようです。 今回、ドイツ・Tübingen大学のDr. Juckerらの研究 …
ピマバンセリン(pimavanserin)
アデュカヌマブの影に隠れていましたが、去年6月、Acadia Pharmaceuticals が抗精神病薬の pimavanserin を認知症の周辺症状の薬として FDA に申請しました。
ガンテネルマブ(gantenerumab)
DIAN-TUコホート第一期で検証されたガンテネルマブ。
一次アウトカムの結果はイマイチでしたが、Aβ、タウ、ニューロフィラメント (NfL) 等のバイオマーカーの結果から、期待される声もあります。
患者さんの副作用は強くなかったので、Roche は用量をあげ、毎週皮下注での効果を検証中とのこと。
ドナネマブ(donanemab)
ソラネツマブが失敗に終わったイーライリリーですが、別のAβ抗体、ドナネマブの臨床試験(Phase 2)を行っています。
BACE阻害薬
多くのBACE阻害薬の治験が中止に終わりましたが……まだ諦めていない製薬会社もいるよう。
どうなるでしょうか?
それ以外の抗Aβ治療薬
上記以外にも続々臨床試験中。
Phase 3
- UB-311
- ALZ-801
- GV-971
Phase 2/3
- azeliragon
- EGCG
Phase 2
- varoglutamstat (PQ912)
抗タウ治療薬
タウは色々な部位でPTMを受けているので、候補となるタウ抗体も様々です。
タウ抗体いろいろ
近年、抗タウ抗体の治験が相次いで開始されましたが……今の所、失敗続き。
今の所ネガティブの結果が出ているタウ抗体療法
- semorinemab (Genentech)
- tilavonemab (Abbvie)
- gosuranemab (Biogen)
タウの中間部位を認識する抗体の抗体療法
上記3つの抗体は、タウのN末をターゲットとしているので、人々の関心は中間部の (proline-rich domain や microtubule binding domain)へ。
- zgotenemab (Lilly)
- JNJ-63733647 (Lilly)
- bepranemab (UCB)
- BIIB076 (Biogen)
- E2814 (Eisai)
- LU-AF87908 (Lundbeck)
能動的タウワクチンの治験
タウワクチンも治験が進んでいます。
- ADDvac1 (Axon Neuroscience)
- ACI-35.30
その他のタウ抗体療法
他、タウオリゴマーを標的とした分子化合物や、アンチセンスオリゴもPhase 1が開始されています。
炎症をターゲットとした治療薬
ADと炎症との関連についても研究が進み、候補治療薬の治験が進められています。
- AL002 (Trem2 antibody, Phase 2)
- inzomelid (NLRP3-containing inflammasome阻害薬)
- pepinemab (semaphorin 4D抗体, グリアのサイトカイン放出を抑制, for HD & AD)
- neflamapimod (p38 MAPK kinase 阻害薬, for DLB & early AD)
シヌクレイノパチーの治療薬候補
シヌクレイノパチーとADは密接に関連しているので、シヌクレイノパチーの治験が進めば、ADにも再配置できるかも……
- prasinezumab (Roche, Phase 2)
- DNL201 (LRRK2阻害薬, Phase 1)
- LTI-201 (GBA活性化薬, Phase 1)
- NPT520-34 (Toll-like receptor 2, Phase 1)
髄液・血液バイオマーカー
Aβ42/Aβ40比の血漿での測定が承認
昨年10月、C2Nの質量分析法ベースのAβ42/Aβ40比測定法が大きく躍進。St. Louisを主とした会社が、結晶測定でCLIAの承認を得ました。
PETよりも安価なので、大変喜ばしい事だと思います。
血漿中タウ
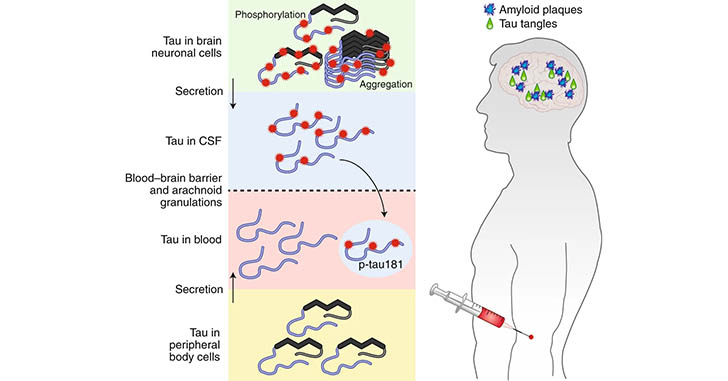
タウのバイオマーカーに関しても、大きな変化がありました。
去年3月、血漿中p-tau181が、脳内のAβプラークとタウタングル量と相関する事が発表され、
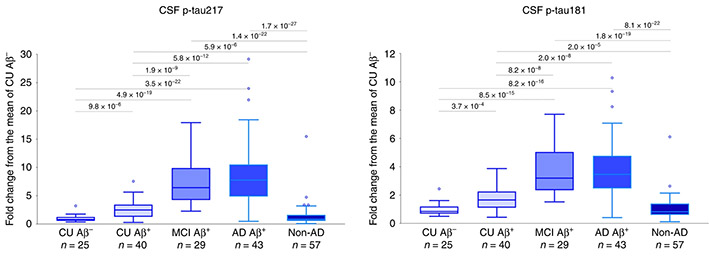
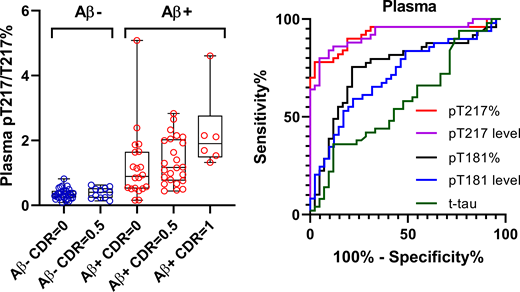
7月、血漿中p-tau217が、血漿中のp-tau181やNfL、イメージングデータよりも感度・特異度が高い、という結果が発表されました。
他には、タウのN末フラグメントのNT1が、タウタングル蓄積、認知機能低下、神経変性と相関する事が報告され、
また、CSF中のタウ微小管結合ドメイン (microtubule binding domain, MTBD) のフラグメントが、PETの結果や認知症症状と相関することも報告されました。
先月のNature Medicineに抱き合わせで発表された、血漿P-tau181に関する報告を2報紹介します。 血漿中P-tau181はADの有望なマーカーとなり得る スウェーデン・Lund 大学からの報告 1つ目の論 …
アルツハイマー病(Alzheimer's disease, AD)のバイオマーカーとして、 血漿中のAβ/タウ/NfLの組み合わせの報告(こちら)、 血漿中のp-tau181の報告(こちら)等、 色々でてきていますが、 …
スペインAugust Pi i Sunyerバイオメディカル研究所のLorenaらの研究グループは、ADバイオマーカーと長期的な認知機能低下について検証した。 対象者:認知機能正常者(cognitively and bi …
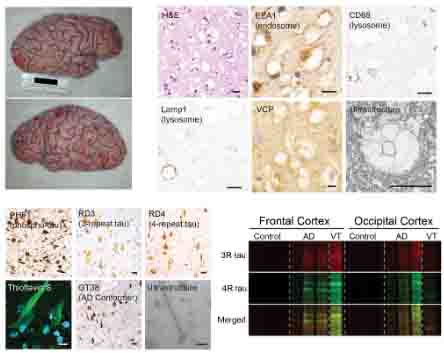
進行性核上性麻痺(Progressive supranuclear palsy, PSP)は、 核上性注視障害、姿勢反射障害による易転倒性、認知症などを主症状とする慢性進行性の変性疾患で、 病理学的には、4リピートタウの …
以前、p-tau181が血漿サンプルで測定可能で、かなりアルツハイマー病(Alzheimer's disease, AD)特異的なバイオマーカーになり得る [1, 2]、という話(こちら)をしました。 また、別のタウリン …
血漿中NfL
血漿中Aβ42やp-tauと同じように、血漿中のNfLも認知機能低下の症状が現れる前から上がっている事が報告されました。
脳脊髄液(cerebrospinal fluid, CSF)中のタウ、ニューロフィラメント(neurofilament light chain, FfL)、アミロイドβ(Aβ)は、アルツハイマー病(Alzheimer's …
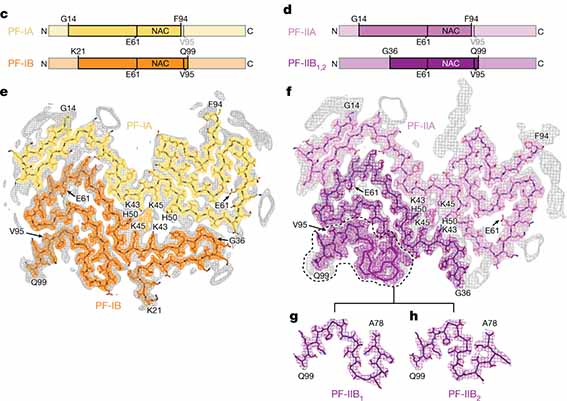
Cryo-EM
昨年も、Cryo-EMを使って、重要な発見がいくつも報告されました。
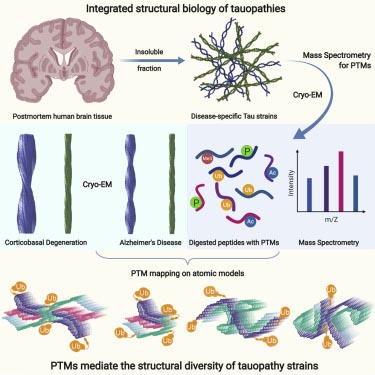
タウでは、大脳皮質基底核変性症 (corticobasal syndrome, CBD) のタウフィブリルの構造がAD, Pick病、CTEなどのタウフィブリルの構造と異なる事が報告され、タウのstrainの違いが、病理や症状の違いを生み出す、という仮説をサポートしました。
シヌクレインでは、多系統萎縮症 (multiple system atrophy, MSA) の患者さんのシヌクレインフィブリルの構造が明らかとなり、
また、昨年はじめて、LRRK2の高次構造が解明されました。
タウオパチーとして分類される疾患(Alzhiemer's disease, AD; Pick's disease, PiD; CBD; Progressive supranuclear palsy, PSP; Chron …
Cryo-EMで前方側頭葉変性症(FLTD), アルツハイマー病(AD), 慢性外傷性脳症(CTE), 大脳皮質基底核変性症(CBD)のタウを次々と解析している、イギリス・MRC Laboratory of Molecu …
また、技術革新も。
昨年10月、2つのグループが、ハードウェアとソフトウェアの改良により、X線結晶構造解析と同レベル (1.2Å) の解像度まで詳細に解析できることを発表。
他のグループは、5量体のGABAA受容体の高次構造を、1.7Å の解像度で解析しました。
イメージング
イメージングの分野も躍進。
タウPET
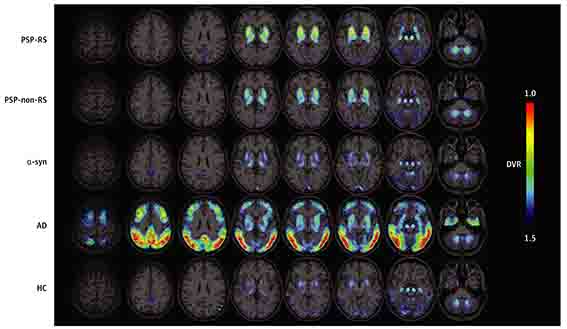
新しいPETトレーサーのJNJ-067 と SNFT-1 が、従来使われている flortaucipir よりも特異的にタングルに結合する事が報告され、昨年5月に FDA の承認を得ました。
より感度の高い MK-6240、4R-tau に特異的に結合し、CBD や 進行性格上性麻痺 (progressive supranuclear palsy, PSP) の診断ツールとして有望な PI-2620 や APN-067 なども報告されました。
また、Roche の RO-498 は、逆に "AD特異的な" タウトレーサーとして注目されています。
他には、タウPETを使って、タウ病理の進展がどうなっているのか、やや controversial な報告もでており、今後の研究報告が望まれます。
アルツハイマー病 (Alzheimer's disease, AD) では、アミロイドβ (Amyloid beta, Aβ) プラークと神経原線維変化 (neurofibrillary tangle, NFT) が病理 …
アミロイドPET
アミロイドPETはまだまだ検査費が高くつくのですが、IDEAS study の結果では、PET を行うことで患者さんの入院率を減らせるのは 5% 程度、という結果がでており、目標値の 10% を大きく割り込みました。
費用対効果の面で見直しが必要のようです。
他のPET
タウPET、アミロイドPET 以外にも、トレーサーが開発されています。
UCB-J はシナプス小胞に結合するトレーサーですが、AD やその他の神経変性疾患の患者さん達の、大脳皮質のシナプス減少をみることができ、タウタングルの蓄積や認知機能低下と逆相関する、と報告されました。
グリア
ミクログリアの動きについて見直しが必要
齧歯類、とくにマウスを使った実験は、神経変性疾患の研究でも重要な位置を占めていますが、全ての細胞や分子の動きが人間と同じだとは限りません。
とくに、ミクログリアに関しては……
昨年1月、TREM2シグナル依存性のアミロイドへのグリアの動きが、マウスとヒトとで異なり、マウスではホメオスタシス遺伝子の発現量が低下するのに対して、ヒトでは上昇する、ということが報告されました。
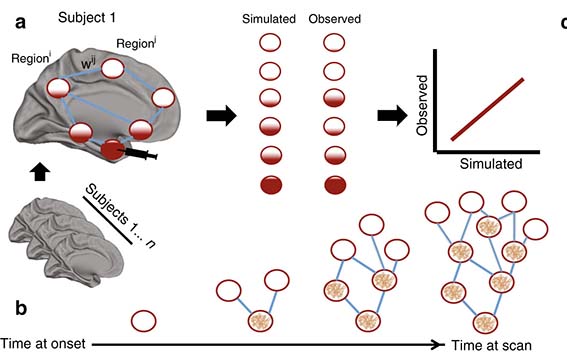
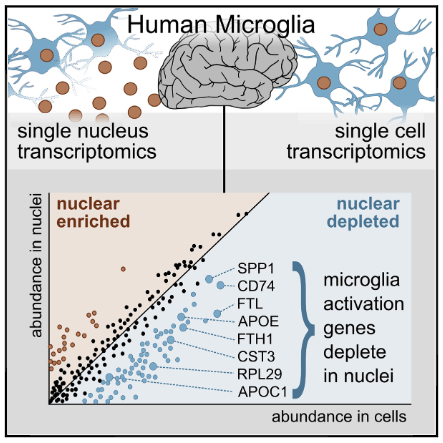
また同年10月には、ADのミクログリアの転写変化は主に細胞質蛋白に多い事から、ヒトの死後凍結脳サンプルを使ってsnRNA-Seqで解析する事に疑問を投げかける研究結果が報告されました。
脳内での細胞達の動向をみるために、シングルセルRNAシークエンス(single-cell RNA-Seq, scRNA-Seq)が注目され、 これまで、マウス脳内やヒト脳内での各細胞のheterogeneityについて多 …
グリアの反応性は、彼らが病変にどれだけ近くにいるかにかかっている、という研究結果も。
spatial transcriptomics と in-situ sequencing を組み合わせて、遺伝子変化は、マウスでもヒトでも、プラークに近い部分でだけ起こっている、という研究結果が報告されました。
最も遺伝子変化が強かったのは、ミクログリアとオリゴデンドロサイトでした。
転写のタイミング
「どこで」だけでなく、「いつ」遺伝子が発現するのかも重要です。
昨年は、"timestamp" RNA と呼ばれる方法が開発され、注目されました。これは、刺激後1時間以内の転写のみをピンポイントで同定することができます。
グリアによるシナプスの刈り込みや死細胞貪食のメカニズムいろいろ
グリアの働きが神経細胞の機能維持等に重要な役割を持つことは疑う余地がなさそうですが、昨年もこれに関するいろいろな研究結果が報告されました。
大規模なプロテオミクス研究では、ミクログリアとオリゴデンドロサイトがAD初期から変化が激しいということが報告されました。
また、ミクログリアはシナプスの刈り込みを行いますが、神経由来の SRPX2 蛋白は C1q をシナプスから遠ざけ、ミクログリアのシナプス刈り込みを遅らせて認知機能低下に寄与してそうだ、という報告もありました。
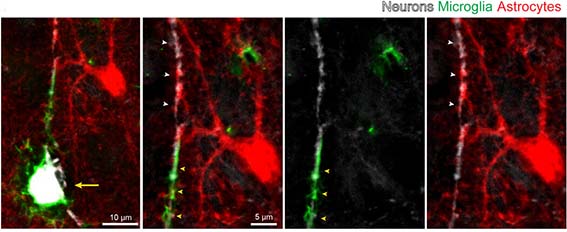
他、AD脳内で神経細胞が死んだあと、ミクログリアとアストロサイトが共同して死細胞の処理にあたっている事も報告されました。
死んだ細胞を処理するのは主にミクログリアと考えられていますが、特殊な環境下ではアストロサイトの貪食も確認されていました 1 。 ニューロンが死ぬ時に出す、"eat-me" シグナルの一つにphosphatidylseri …
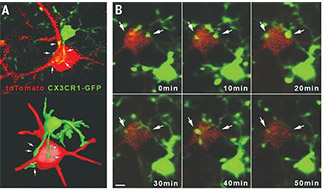
ミクログリアは、脳卒中、てんかん、精神疾患、神経変性疾患etc.、あらゆる病態において重要な役割を担っている。 ハンガリーのCserépら(Ádám Dénesのグループ)は、マウスやヒトの脳内で、ミクログリアが独特の動 …
血管系
ADにおける血管系の役割も、毎年新しい研究結果が報告されています。
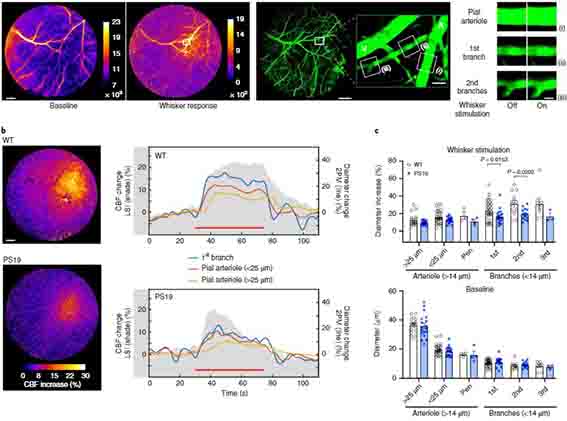
そのうちの1つは、タウが血流調節にも関与していそうだ、という報告。
脳内には、神経活動の量に合わせて、局所の血流があがる Neurovascular Coupling (NVC) というシステムがあります。 高齢者の方や、アルツハイマー病(Alzheimer's disease, AD) …
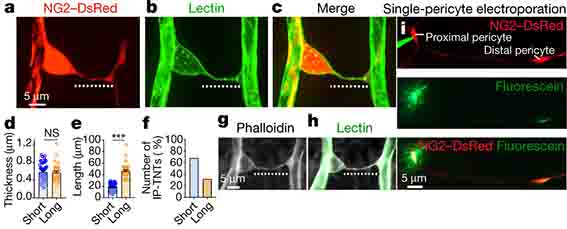
他には、毛細血管上のペリサイトが、ナノチューブでお互いつながり、協調して毛細血管の血流調節を行っているようだ、という報告もありました。
細胞間同士のナノチューブの存在は、in vitroやex vivoの実験で以前から指摘されていましたが、 今回、カナダ・モンテリオール大学のAlarcon-Martinezらの研究グループは、 マウスの網膜と脳内でペリサ …
ペリサイトの血流調節には、色々議論が交わされてきましたが、やっぱり毛細血管の血流調節に複雑に関与しているようです。
最近、ある総論を書いているのですが、レビューアーとやり取りをしながらちょっと切なくなっていているので、その理由を徒然なるままに書いてみます。 総論の内容 ペリサイトについて 総論は、ペリサイト(pericyte, 周皮細 …
脳血流(Cerebral blood flow: CBF)は神経活動によって巧みに変化し、Neurovascular couplingと呼ばれる。 デンマーク・コペンハーゲン大学のGrubb、Lauritzenらのグルー …
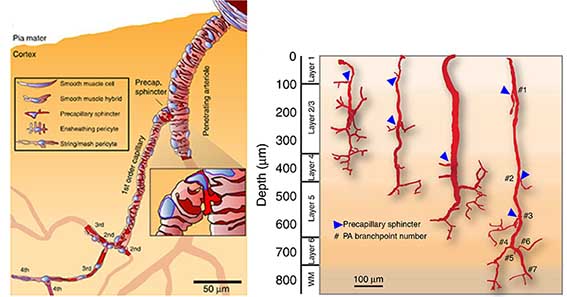
もう少し大きな血管、細動脈では、内皮細胞の calveolae が神経活動に合わせて脳細動脈の血流調節を行っている、という報告もありました。
ジェネティックス
2020年は、ジェネティックス研究にとって当たり年と言えそう、とのこと。
ただAD関連遺伝子を見つけるだけでなく、それらがどのように機能して病態に関与しているのかを詳細に解析できるようになっています。
GWAS
一方で、今年はアフリカン・アメリカンを対象とした GWAS で、insulin-like growth factor receptor 遺伝子や RBFOX1 近くの遺伝子などの多型が新たにリスク多型として同定されました。
他にも、RNA-binding protein 遺伝子がアミロイドーシスと関連する、という GWAS 研究も報告されました。
このブログでは取り上げませんでしたが、angiotensin-converting enzyme (ACE) 遺伝子の多型が AD のリスクとして浮上しました。
ACE といえば血圧ですが、この変異は血圧とは独立して、神経変性に関与するそうです。
また別の論文では、valosin-containing protein (VCP) 遺伝子の変異で、タウ凝集体分解機能の低下により、家族性前頭側頭葉変性症(Frontotemporal lober degeneration, FTLD)を発症する、ということも報告されました。
valosin-containing protein (VCP) は、全ての真核生物と古細菌などに存在するATPaseで、 ユビキチン-プロテアソーム系(Ubiquitin-proteasome system, UPS) …
他には、家族性パーキンソン病 (Parkinson's disease, PC) の原因遺伝子の一つ LRRK2 が、PSP 発症に関与する、という報告もありました。
機能解析
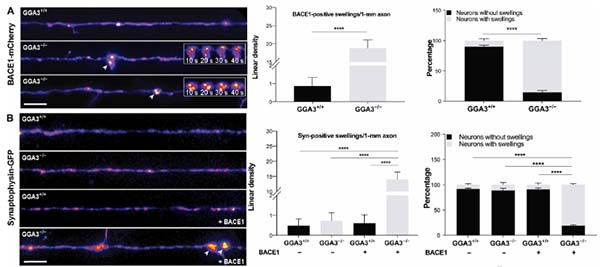
機能解析としては、GGA3 の遺伝子多型で BACE1 の軸索輸送が障害され、腫大した軸索内にAβがたまる、という報告や、
GGA3は、Golgi-localized, gamma adaptin ear-containing, ARF-binding (GGA) ファミリーの一つで、トランス・ゴルジネットワーク–リソソーム間や、エンドソーム …
ApoE4でアストロサイトのエンドサイトーシスが停滞し、PICALM の発現上昇によりそれを改善できる、という報告、
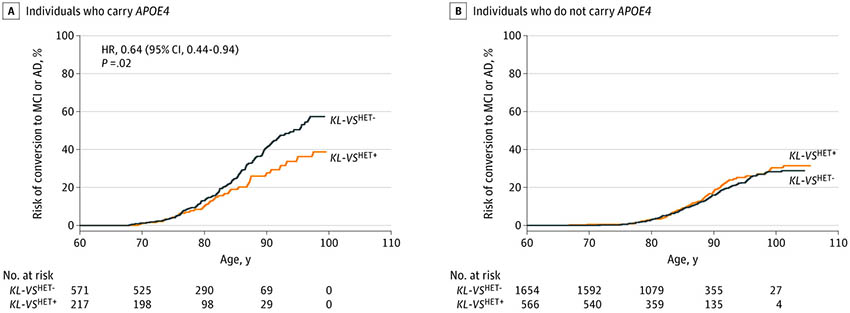
長寿関連遺伝子 Klotho の多型により、プラークがあっても認知機能が維持できる、という報告もありました。
Kotho (KL) は、寿命に関わる膜タンパクとして注目されている。 F352V (rs9536314) とC370S (rs9527025) の二つのミスセンス変異は、機能的ハプロタイプKL-VSとして知られており、 …
phospholipase Cγ2 が TREM2 の下流にあり、ミクログリアの貪食機能等をアップさせているようですが、別の研究では、PLCγ2 は、toll-like receptors 経路で炎症を惹起するという報告もありました。
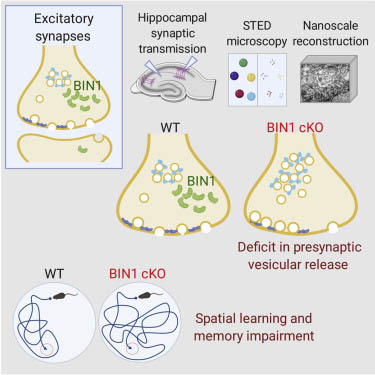
Bin1 はニューロトランスミッターとシナプスの維持に重要である、という研究報告や、
Bridging integrator 1(BIN1)は、BAR adaptor protein familyのメンバーで、late-onset Alzheimer disease (AD)のリスク因子であり、Aβ産生、 …
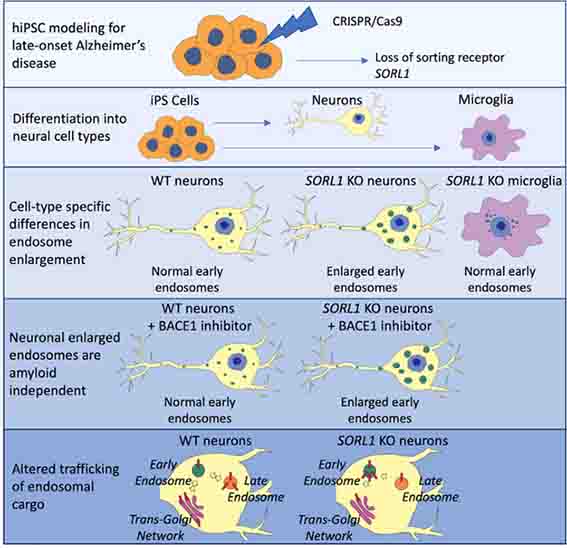
SORL1の機能障害でエンドソームが膨らみ、Aβ産生↑ が起こる、という報告もありました。
アルツハイマー病 (Alzheimer's disease, AD) では、 アミロイドβ (Amyloid beta, Aβ)の凝集・沈着 タウの細胞内凝集 が2大病理ですが、 細胞内病理の一つとして、エンドソームの膨 …
エピジェネティックス
エピジェネティックス関連も多数報告がありました。
DNA demethylase 10-11 translocation 2 (TET2) の変異で、AD と FTD のリスクを2倍になること、
BAZ-2 (修飾されたhistonesに転写因子を動員させる) と SET-6 (histone3/lysine9 methyltransferase) の発現量が加齢とともにあがり、ミトコンドリアの遺伝子発現を抑制して認知機能低下を促進することなどが報告されました。
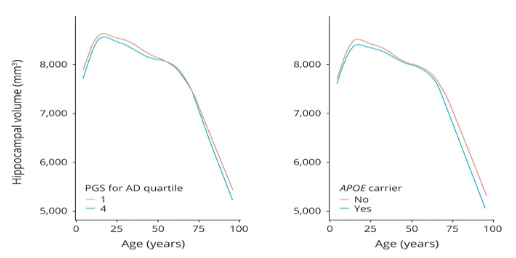
他には、AD のリスク因子がいくつかあると、若い頃から海馬のボリュームに影響があること、
アルツハイマー病(Alzheimer's disease, AD)には、これまで多くのリスク遺伝子が報告されており、特にAPOE4は最も強力なリスク多型と言われています。 ADのリスク遺伝子ランキング(Alzform/T …
遺伝子多型の影響が男女間で異なること、などの報告がありました。
後者に関しては、本来発現が抑えられているはずの2番めのX染色体が、AD病理耐性の方向に働いているようです。
大気汚染
大気汚染は、呼吸器系や心血管系だけでなく、神経変性疾患にも影響がありそうです。
アミロイドPETでAβ蓄積が多い患者さんの数は、PM2.5の量が多い地域に密集し、その相関度は呼吸器系癌の患者数との相関よりも高かったとのこと。
別の研究では、9.11 後の World Trade Center を清掃した人たちが、50歳代で認知症の症状を多く発症しているとのこと……因果関係は「ほんとかな?」と思ってしまいますが……フォローしていくと見えてくるものがあるかもしれません。
ADは感染症?
異常凝集したタウが脳内を伝播する……と聞くと、「プリオンみたいに感染するの?」と思ってしまいます。
プリオンみたいにわっと感染することはないですが、以前ヒト成長ホルモン投与によりAβが伝播した可能性を示唆する論文も出ており、
著者らは、以前、死後脳の下垂体から抽出・精製したヒト由来成長ホルモン(human cadaveric pituritary-derived grouth hormone:c-hGH)投与により、医原性クロイツフェルト・ヤ …
本当の所はどうなのか、心配する人も少なからずいるようです。
このような背景を受けて、昨年、手術器具等で病的蛋白が感染したとする、過去の報告をまとめた論文がでました。
以前、死後脳の下垂体から抽出・精製したヒト由来成長ホルモン(human cadaveric pituritary-derived grouth hormone:c-hGH)投与が原因で、数年~数十年後に脳アミロイドーシス …
今の所、手術器具等を介してAβ、タウ、シヌクレインのような蛋白が感染した、という明確なエビデンスはなく、過度に心配しないほうが良い、というのが当局の見解になっています。
まとめ
以上、Alzforum で発表された「2020年の内容と2021年の展望について」でした。
昨年は、研究の世界も COVID-19 一色で、手を動かしての研究ができない人が多かったですが、データ整理など、できることを進め、世界の研究全般としては、大きな遅れにはならなかったようです。
今、私の務める大学病院には、COVID-19 ワクチンが続々と届いており、優先順位の高い人達からワクチン接種が始まっています。
新規のワクチンということで、実際に接種するのは怖いですが……順番が回ってきたら、接種しようと……でも、やっぱり怖いな……