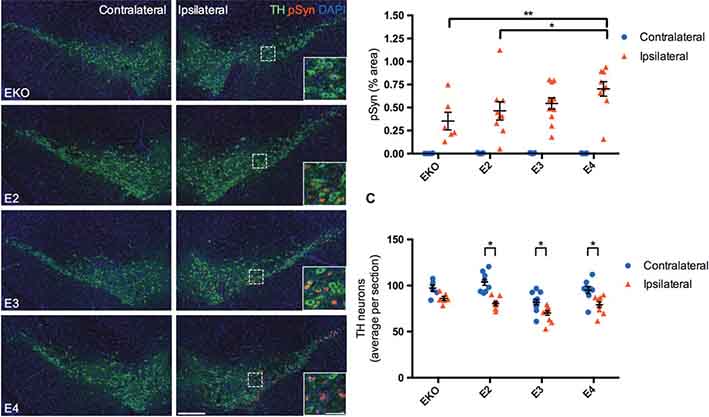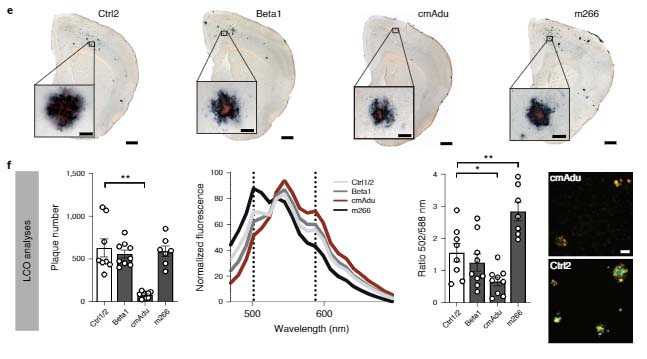
先月6日に行われたFDAのアデュカヌマブミーティングではだいぶ旗色が悪く、FDA承認は難しそうな印象ですが、
少なくともマウス脳内では成績優秀のようです。
今回、ドイツ・Tübingen大学のDr. Juckerらの研究グループは、アミロイドβ(Amyloid beta, Aβ)プラークができる初期の段階からアデュカヌマブを接種すると、
晩年のAβプラーク病理形成が抑えられる、という内容を報告しました [1]。
アデュカヌマブの効果はずっと続く?
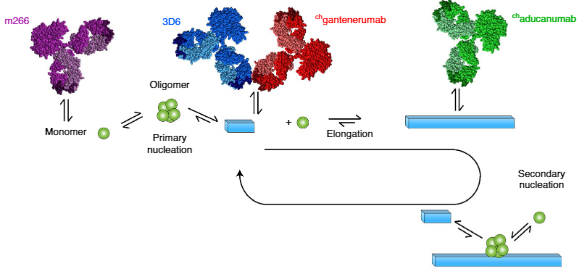
著者らは、各種Aβ抗体
- Beta1
- cmAducanumab(アデュカヌマブ)
- cmGantenerumab(ガンテネルマブ)
- m266(ソラネズマブ)
- mC2(クレネズマブ)
- mE8(ドナネマブ)
を、6ヶ月齢のAPP23マウスに、毎日5日間接種し、1ヶ月半後に脳内の可溶性/不溶性Aβ量、Aβプラーク量を確認したところ、
アデュカヌマブ接種群でAβプラークの量が減少していた。
それぞれの抗体がAβプラークの基となるAβシードのどの部分を認識するのか調べるため、
著者らは、それぞれの抗体のシード認識部位を、antibody recognition profiling of Aβ assemblies (ARPA) という方法で検証した。
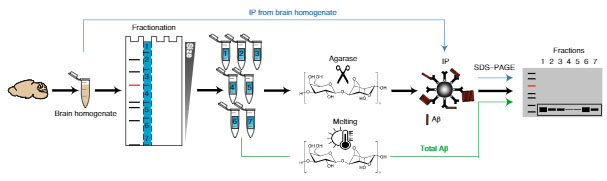
<ARPAの方法>
- APP23マウスの脳のPBS画分をそれぞれの抗体で免疫沈降 (IP)し、アガロースゲルで電気泳動
- ゲル上のAβ集合体を、任意の大きさで切り取り、それぞれのAβ抗体でIP
- 各画分を電気泳動し、各抗体がどの画分のAβ集合体を最も認識するか確認
結果、アデュカヌマブはより大きな画分のAβシードをキャプチャーすることがわかった。
著者らは、この大きなAβシードブロッキング作用により、アデュカヌマブが長期的なAβプラーク形成を抑制するかどうか調べた。
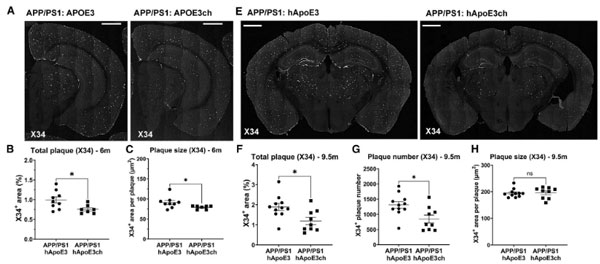
6ヶ月齢のAPP23マウスとWTマウスにBeta1、ソラネズマブ、アデュカヌマブを接種し、その6ヶ月後(12ヶ月齢)に観察したところ、
アデュカヌマブは不溶性Aβ量やAβプラークの数が減少しており、neuritic plaqueやグリアの増生も抑えられていた。
以上の結果から、アデュカヌマブは、
Aβ凝集過程の極初期に投与
↓
最もpotentなAβシードをブロック
↓
以降のAβ凝集体形成を阻害
というメカニズムで、後々まで効果が持続する可能性が示唆された。
My View
以前、治験に使用されている各種Aβ抗体の、Aβ凝集過程における阻害部位が違うという事をvitroで検証した論文を紹介しましたが、
1999年にSchenkらの研究グループがアミロイドβ(Amyloid beta, Aβ)抗体による、ADモデルマウス脳内のAβプラーク消失と認知機能改善を報告 [1] して以来、現在まで多くのAβ抗体が開発され、臨床応 …
今回は、それをvivoでも証明するような内容の論文でした。
今回の研究ではAβのプロトフィブリルに結合するBAN2401は含まれていなかったので、それもみてみたいところです。
ARPAという方法は新しく、正直ちょっとしっくりこないところもあったのですが、
私の中では、
「大きな画分のAβ集合体は小さな画分のAβ集合体とは違う構造をとっていて*注1、アデュカヌマブが認識する構造のAβ集合体の方がシード能が高い、ということなー」
(*注1. 例えば、大きな画分のAβ集合体では隠れているような部位が、小さな集合体では切断→露出されているとか、Aβが特定のオリゴマー構造をとったところにポイントがある 等々……)
と認識しています。
(間違っていたら指摘してください。)
APP23マウスは、スウェーデン変異のAPPTgマウスで、7倍のAPP発現量があり、6ヶ月齢ごろから少しずつAβプラークが出現します [2]。
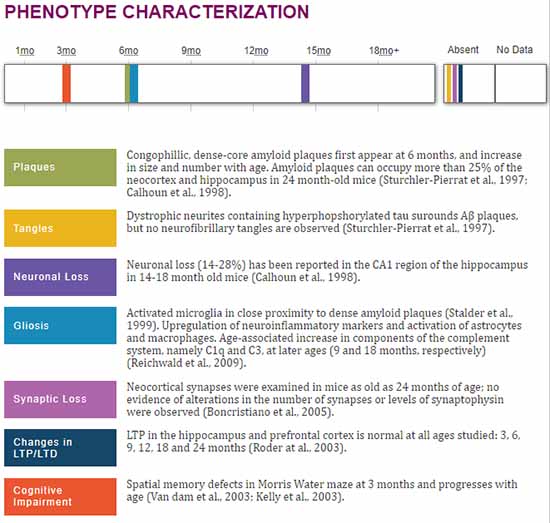
今回6ヶ月齢から投与して12ヶ月齢で観察しているので、人だとアルツハイマー病(AD)と診断される20年以上前からアデュカヌマブを投与しておく必要がある、ということでしょうか。
DIAN研究の結果からは絶対効果ありとは言い切れない気もしますが、
変異のない人達の集団で、40歳くらいの人たちにアデュカヌマブを数回投与してみて、30年後にどれくらいの人達がADを発症するかといった感じの臨床研究が組めれば、結果がでる……かもしれません。
でも、現実的には難しいかな。
気になったのは、
長期的にAβプラークが減少することはわかったけれども、それで認知機能低下まで抑えられているのかどうか、というところ。
APP23マウスは3ヶ月齢くらいから認知機能障害が出て、年齢依存的に増悪するようなので、見ようと思えば見れたはずだと思うのですが。
まあ、マウスだと認知機能は改善してそうですけど……
References
- Uhlmann, R.E., Rother, C., Rasmussen, J. et al. Acute targeting of pre-amyloid seeds in transgenic mice reduces Alzheimer-like pathology later in life. Nat Neurosci 23, 1580–1588 (2020). https://doi.org/10.1038/s41593-020-00737-w
- APP23 | ALZFORUM