運動の認知機能等に対する効果については、このブログでも何度かとりあげてきました。
運動が認知機能に良い影響をもたらすという研究結果は多数報告されている。 インスリン、レプチン、GLP1、グルココルチコイドなど、中枢神経以外で産生されるホルモンが神経保護やシナプスの可塑性などを介して、認知機能向上を促す …
運動がアルツハイマー病などの認知症予防に効果的であることは、このブログでも何度かとりあげました。 機序的にも疫学的にも、運動の認知機能に対するポジティブな効果は疑いようがないんじゃないかと思います。 でも運動の効果って、 …
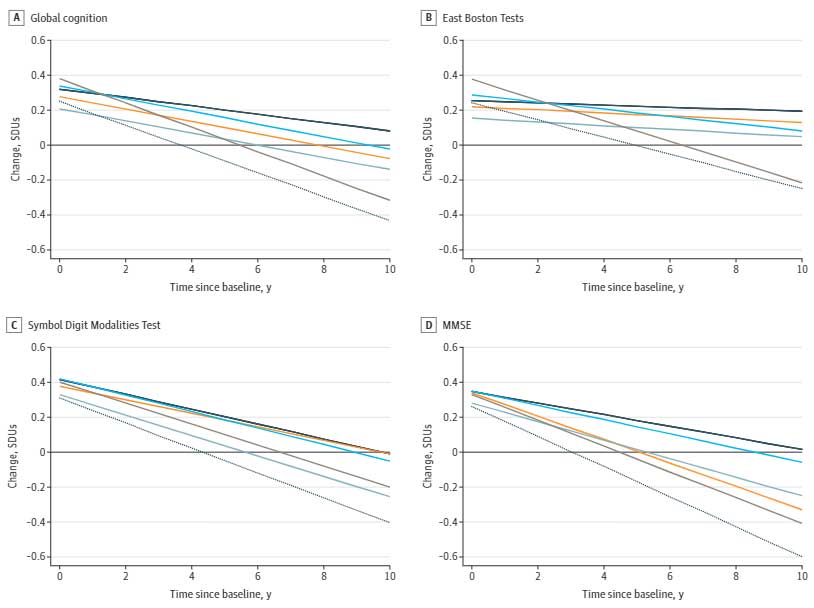
運動が、身体だけでなく、脳機能や精神の健康維持にも欠かせないのは周知の事実ですが、実際、どれくらいの運動で効果があるのでしょうか? ドイツ・ハイゼンベルグ大学のDr. Meyer-Lindenbergらの研究グループは、 …
運動がアルツハイマー病(Alzheimer's disease, AD)などの変性疾患病理を抑えたり神経新生を促したりして、認知機能を保つ効果がある事については多くのエビデンスがありますが、
そのメカニズムは一つではなく、複数の機序がシナジー的に効力を発揮していると考えられます。
その中でも主流となっているメカニズムの一つが、
「運動によって末梢で産生亢進したファクターがBBBを通り抜けて脳内に届き、神経新生などに寄与する」
今回、アメリカ・スタンフォード大学の Dr. Wyss-Coray らの研究グループからの報告もその一つになると思います。
彼らは、
「運動すると、血漿中のクラステリン(clusterin, CLU)の濃度があがり、それが脳に届いて神経炎症を抑える。」
という事を報告しました [5] 。

運動すると血漿中のクラステリンによって脳の炎症が抑えられ、認知機能がUPする
運動したマウスの血漿を注入すると、認知機能がUPする
著者らは、
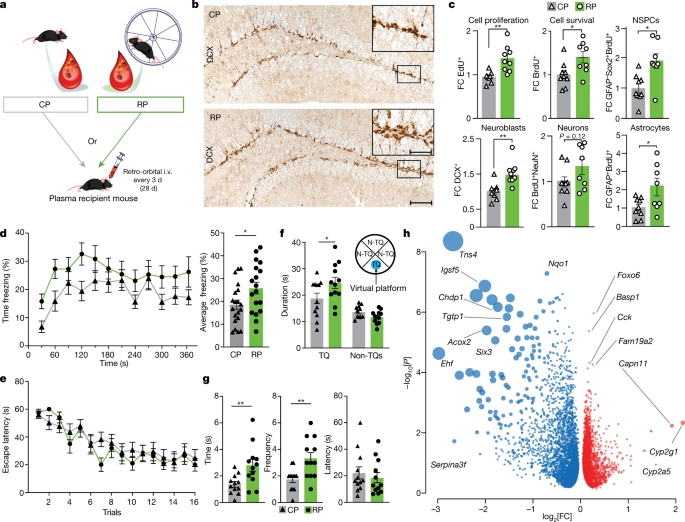
- running wheel で運動をさせたマウスから採取した血漿(running plasma, RP)
- じっとしているマウス(control plasma, CP)
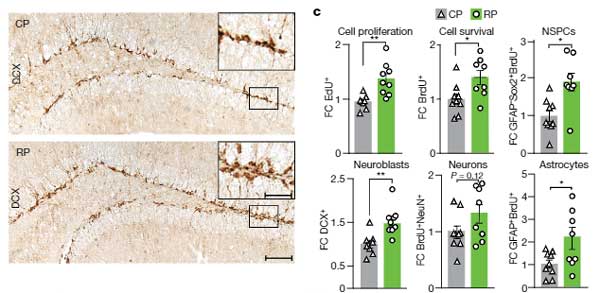
を、それぞれ別のマウスに注入し、その後の海馬の様子や認知機能などを調べました。
すると、RP を注入したマウスの海馬では神経新生などが増えており、
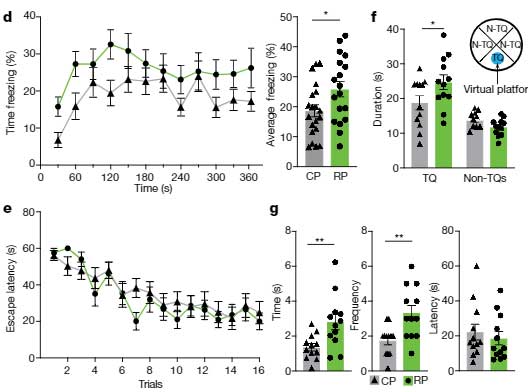
認知機能も良くなっていました。
RP, CP, 生食をそれぞれ注入したマウスの海馬でRNAシークエンスを行うと、RP 注入マウスでは
- 細胞の遊走 (Tns4)
- 細胞接着 (lgsf5)
- 内皮細胞の増殖や分化 (Ehf)
などの遺伝子発現が下がり、
- 海馬の学習機能や記憶に関連する遺伝子 (Foxo6)
- 免疫や神経可塑性に関連する遺伝子 (Fam9a2)
などの発現が上がっていました。

以上の結果から、
「実際に運動しなくても、運動したマウスの血漿成分を注入する事で、神経新生や認知機能UPという運動の効果を再現できる」
という事が示唆されました。
運動したマウスの血漿成分は、脳内の神経炎症を抑える
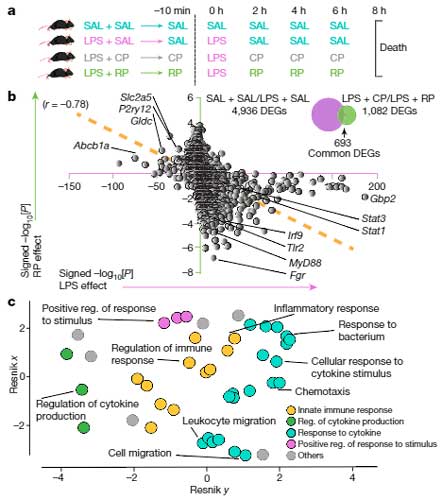
RP の効果を調べるため、著者らは lipopolysaccharide (LPS) を末梢血から注入して脳内炎症を誘導し、その状態で RP と CP を注入しました。
結果、RP 注入マウスでは、
- toll-like receptor (TLR) シグナル経路 (Myd99, Tlr1, Tlr2, lrak3 etc.)
- インターフェロン経路 (lrf9, lnfgr1, Stat1, Stat3 etc.)
- アストロサイト活性化 (Gfap)
などの炎症系の遺伝子発現が抑えられていました。
運動したマウスの血漿は、補体や血液凝固系経路を変化させる
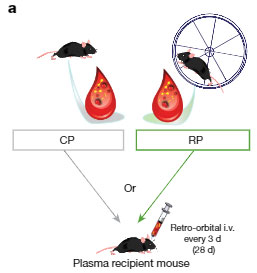
著者らは RP と CP で変化しているタンパクを
- unbiased shortgun mass spectrometry (MS)
- tandem mass tag (TMT) isobaric labelling of proteins
- synchronous precursor selection-based MS3 (SPS-MS3) MS
で調べました。
すると、
- H因子 (factor H, FH)
- 補体因子C3aとC5a
など、補体系および凝固系の経路に属するタンパク群が変化しており、
特に、
- クラステリン (clusterin, CLU)
- 補体因子H (complement factor H, FH)
- 補体1阻害因子 (C1INH)
- 膜侵襲複合体 (membrane-attack complex, MAC) のC8
などがRPで上昇していました。

クラステリンが運動による脳抗炎症作用の主因子
RP の抗炎症作用に最も強い影響を与えているファクターを探るため、MSで変化が確認されたタンパクのうち、
- CLU (抗炎症作用。多型はADのリスク多型にも。心疾患に保護的に働く。)
- FH (補体系および凝固系カスケードに関与。)
- PEDF (glucoprotein pigment epithelium-derived factor。抗炎症作用。)
- LIFR (leukaemia inhibitory factor receptor。抗炎症作用。)
を免疫沈降で除去して、LPS注入マウスに接種してみました。
すると、CLUを除去したRPでは脳内の抗炎症効果が著しく低下しており、
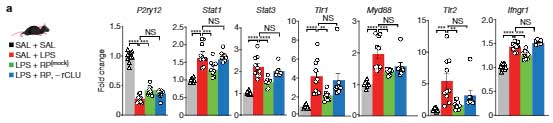
「運動による血漿中のクラステリンが、脳内の抗炎症に最も大きく作用している」
という事がわかりました。
蛍光標識したリコンビナントCLUを血管内に注入すると、CLUが内皮細胞に結合して脳内に取り込まれている様子が観察されている様子が観察されました。
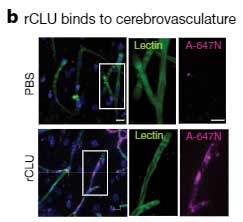
APPマウスでもクラステリンによる抗炎症作用を確認
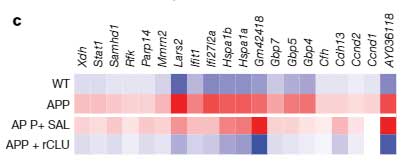
自然と神経炎症が起こるマウスでもCLUの効果を確認するため、Thy1プロモーターに変異APP遺伝子を組み込んだマウス(mThy-hAPP751V171I, KM670/671NL;T41 line; 17 mo)17ヶ月齢にリコンビナントCLUを注入して遺伝子発現変化を調べました。
すると、RPがLBPによる脳内炎症を抑えたのと同じ用に、老齢APPマウスの神経炎症もリコンビナントCLUで抑える事ができました。
運動をした人の血漿中でも同様の変化を確認
最後に、軽度認知機能障害 (amnestic micl cognitive impairment, MCI) の患者さんに6ヶ月間運動をしてもらって、運動をすると本当に上記のタンパク群が変化するのか調べました。
結果、CLU↑、FX↓、C3↓、FII/プロトロンビン↓、uPA↓、プラスミノーゲン↓ など、運動マウスの血漿とほぼほぼ同様の効果が得られ、
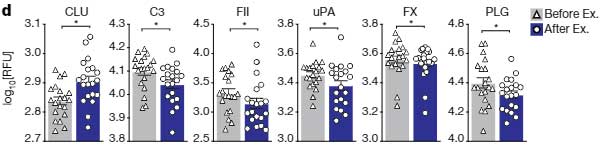
「人でも運動によって血漿中のCLUが上昇し、脳内炎症を抑えたり神経新生を促したりする」
という可能性が示唆されました。
Plasma from voluntarily running mice reduces baseline expression of neuroinflammatory genes and experimentally induced brain inflammation when infused into sedentary mice.
My View
という事で、今回は、
「運動により血漿中のクラステリン量が上がり、それが脳内に移行して神経炎症を抑え、もしかしたら神経新生などにも関与して認知機能がよくなるかも。」
という内容でした。
クラステリンの遺伝子多型のいくつかはアルツハイマー病(Alzheimer's disease, AD)のリスク多型にもなっており (Glossary参照)、
AD患者さんの末梢血へのクラステリン投与が脳内に良い影響を及ぼす可能性も示唆されているように思います。
クラステリンの受容体は内皮細胞に多く発現しているようなので [6] 、末梢から脳内に移行できる、というのは魅力ですね。
ただ、ADやMCIの患者さん脳内ではクラステリン量が既に上がっているという報告もあります [7]。
代償的に上がっていると考える事もできますが、それにプラスして更にクラステリンを投与して、どれくらい効果が得られるかなー、という気持ちにもなります。
でも、もっとクラスリンUPしたら効果が得られる、という事になるかもしれないし、トライする価値はあるかもですね。
Glossary
| ADのリスク遺伝子ランキング(Alzform/TopResults.asp [1] より) | |||||
| # | Gene | |
Ethnicity | |
|
| 1 | APOE | APOE_e2/3/4 | All | 3.685 (3.30-4.12) | <1E-50 |
| 2 | BIN1 | rs744373 | All | 1.166 (1.13-1.20) | 1.59E-26 |
| 3 | CLU | rs11136000 | Caucasian | 0.879 (0.86-0.90) | 3.37E-23 |
| 4 | ABCA7 | rs3764650 | All | 1.229 (1.18-1.28) | 8.17E-22 |
| 5 | CR1 | rs3818361 | Caucasian | 1.174 (1.14-1.21) | 4.72E-21 |
| 6 | PICALM | rs3851179 | Caucasian | 0.879 (0.86-0.9) | 2.85E-20 |
| 7 | MS4A6A | rs610932 | All | 0.904 (0.88-0.93) | 1.81E-11 |
| 8 | CD33 | rs3865444 | All | 0.893 (0.86-0.93) | 2.04E-10 |
| 9 | MS4A4E | rs670139 | All | 1.079 (1.05-1.11) | 9.51E-10 |
| 10 | CD2AP | rs9349407 | All | 1.117 (1.08-1.16) | 2.75E-09 |
References
- Lourenco MV, Frozza RL, de Freitas GB, Zhang H, Kincheski GC, Ribeiro FC, Gonçalves RA, Clarke JR, Beckman D, Staniszewski A, Berman H, Guerra LA, Forny-Germano L, Meier S, Wilcock DM, de Souza JM, Alves-Leon S, Prado VF, Prado MAM, Abisambra JF, Tovar-Moll F, Mattos P, Arancio O, Ferreira ST, De Felice FG. Exercise-linked FNDC5/irisin rescues synaptic plasticity and memory defects in Alzheimer's models. Nat Med. 2019 Jan;25(1):165-175. doi: 10.1038/s41591-018-0275-4. Epub 2019 Jan 7. PMID: 30617325; PMCID: PMC6327967.
- Trejo JL, Carro E, Torres-Aleman I. Circulating insulin-like growth factor I mediates exercise-induced increases in the number of new neurons in the adult hippocampus. J Neurosci. 2001 Mar 1;21(5):1628-34. doi: 10.1523/JNEUROSCI.21-05-01628.2001. PMID: 11222653; PMCID: PMC6762955.
- Fabel K, Fabel K, Tam B, Kaufer D, Baiker A, Simmons N, Kuo CJ, Palmer TD. VEGF is necessary for exercise-induced adult hippocampal neurogenesis. Eur J Neurosci. 2003 Nov;18(10):2803-12. doi: 10.1111/j.1460-9568.2003.03041.x. PMID: 14656329.
- Leiter O, Seidemann S, Overall RW, Ramasz B, Rund N, Schallenberg S, Grinenko T, Wielockx B, Kempermann G, Walker TL. Exercise-Induced Activated Platelets Increase Adult Hippocampal Precursor Proliferation and Promote Neuronal Differentiation. Stem Cell Reports. 2019 Apr 9;12(4):667-679. doi: 10.1016/j.stemcr.2019.02.009. Epub 2019 Mar 21. PMID: 30905740; PMCID: PMC6450435.
- De Miguel Z, Khoury N, Betley MJ, Lehallier B, Willoughby D, Olsson N, Yang AC, Hahn O, Lu N, Vest RT, Bonanno LN, Yerra L, Zhang L, Saw NL, Fairchild JK, Lee D, Zhang H, McAlpine PL, Contrepois K, Shamloo M, Elias JE, Rando TA, Wyss-Coray T. Exercise plasma boosts memory and dampens brain inflammation via clusterin. Nature. 2021 Dec;600(7889):494-499. doi: 10.1038/s41586-021-04183-x. Epub 2021 Dec 8. PMID: 34880498.
- Pohlkamp T, Wasser CR, Herz J. Functional Roles of the Interaction of APP and Lipoprotein Receptors. Front Mol Neurosci. 2017 Mar 1;10:54. doi: 10.3389/fnmol.2017.00054. PMID: 28298885; PMCID: PMC5331069.
- Hsu JL, Lee WJ, Liao YC, Lirng JF, Wang SJ, Fuh JL. Plasma biomarkers are associated with agitation and regional brain atrophy in Alzheimer's disease. Sci Rep. 2017 Jul 11;7(1):5035. doi: 10.1038/s41598-017-05390-1. PMID: 28698646; PMCID: PMC5506051.