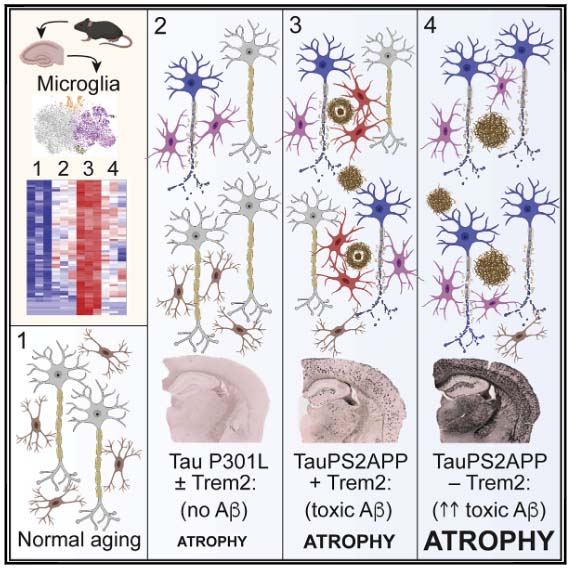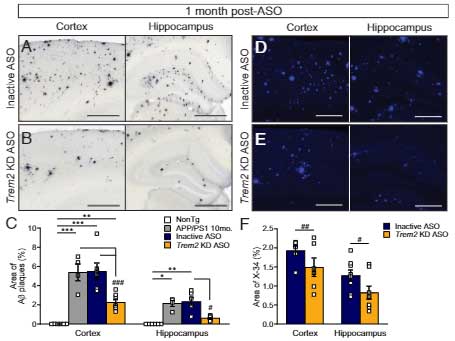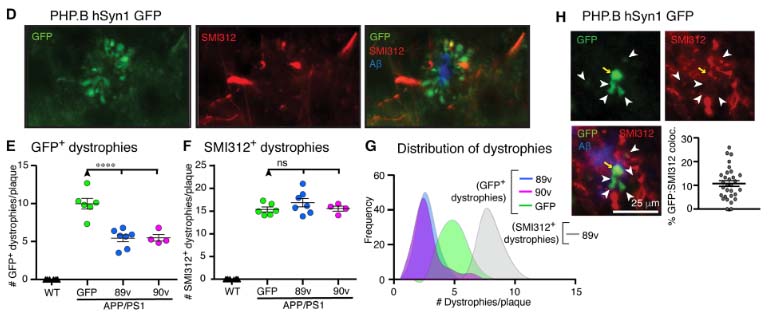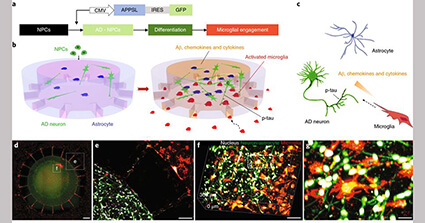
TREM2 (triggering receptor expressed on myeloid cell 2) は、脳内では主にミクログリアに発現する膜貫通型の糖蛋白です。
このTREM2をコードする遺伝子TREM2の点変異はアルツハイマー病 (Alzheimer's disease, AD) のリスク遺伝子で、この変異をヘテロで持つ人達は、low-of-function で約3倍 AD になりやすいといわれています [1, 2]。
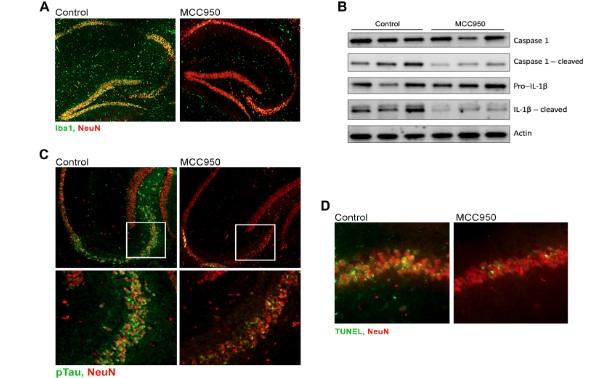
マウスの研究では、 TREM2を欠失させるとミクログリアの貪食機能 etc. が落ちて、Aβ プラークが大きくなり [3, 4]、タウ病理が広がり [5]、神経障害が起こります [6]。
TREM2 (triggering receptor expressed on myeloid cells 2) は、脳内ミクログリアに発現するレセプタータンパク [1, 2]で、この遺伝子の変異はアルツハイマー病 (A …
TREM2 (triggering receptor expressed on myeloid cell 2) は、アルツハイマー病 (Alzheimer's disease, AD) のリスク遺伝子の一つで、 TREM …
このTREM2、Aβ研究では欠かせないADAM familyで切断されて可溶性TREM2(soluble TREM2, sTREM2)を細胞外に放出し、CSF中にも出てきます [6]。
これまで、TREM2変異の患者さんのCSF中ではsTREM2が減っている事 [8]、 TREM2変異のない家族性および孤発性ADさんのCSF中では発症前や極初期の段階から増えている事 [9, 10, 11, 12] などが報告され、
CSF中sTREM2はADのバイオマーカーとして有用であると考えられてきました。
そんなCSF中sTREM2を、経時変化や他のバイオマーカーとの対比などの側面から観察してみると、「ミクログリア vs AD病理」という脳内バトルの状況を垣間見られる……のかもしれません。
今回、ドイツ・German Center for Neurodegenerative Diseases (DZNE) のDr. Morenas-Rodríguez, Dr. Haassらの研究グループは、常染色体顕性遺伝の家族性ADスタディ(Dominantly Inherited Alzheimer Network, DIAN study)に参加するPSEN1, PSEN2, APP変異を持つ方々のCSF中の経時変化およびAβやタウのバイオマーカーとの比較について報告しました [13] 。

CSF中sTREM2から、ミクログリアの善戦の跡を垣間見る
彼らは、2008年から始まったDIANスタディ(Dominantly Inherited Alzheimer Network Study; アメリカ、アルゼンチン、オーストラリア、ドイツ、スペイン、イギリスの17施設)に参加している、PSEN1, PSEN2, APPの変異を持つ方々を
- ノンキャリア(Non-carriers)
- 発症前キャリア(Presymptomatic carriers)
- 発症キャリア(Symptomatic carriers)
の3群に分け、それぞれ
- CSF
- sTREM2
- Aβ24とAβ40
- 全長タウ(t-tau)
- リン酸化タウ181(p-tau)
- 画像
- MRI
- アミロイドPET(11C-PiB)
などを縦断的に調べました。
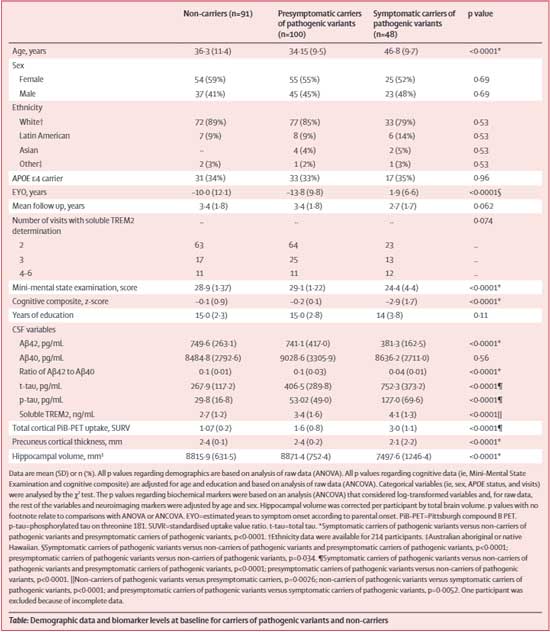
CSF中sTREM2はPSEN1/PSEN2/APPキャリアで上がっている
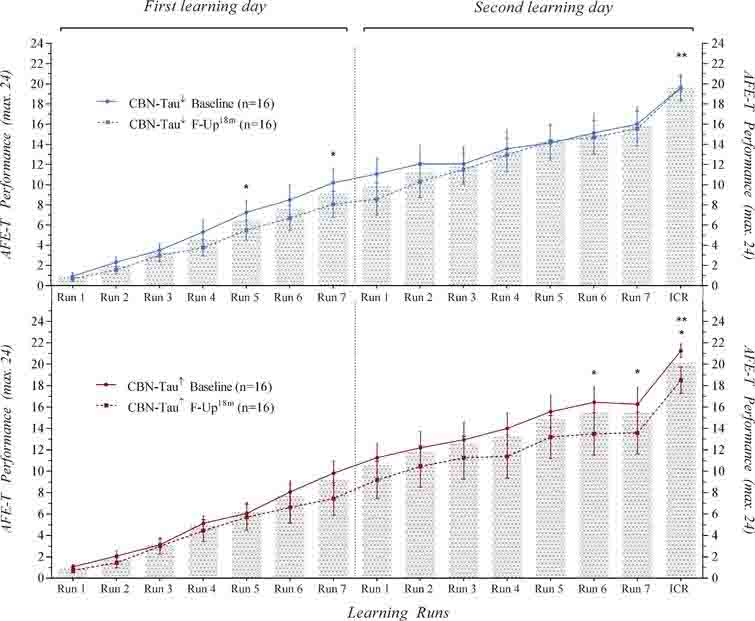
CSF中のsTREM2濃度を経時的に調べると、全期間を通して、CSF中sTREM2濃度はキャリアの人達の方がノンキャリアよりも高くなっていました。
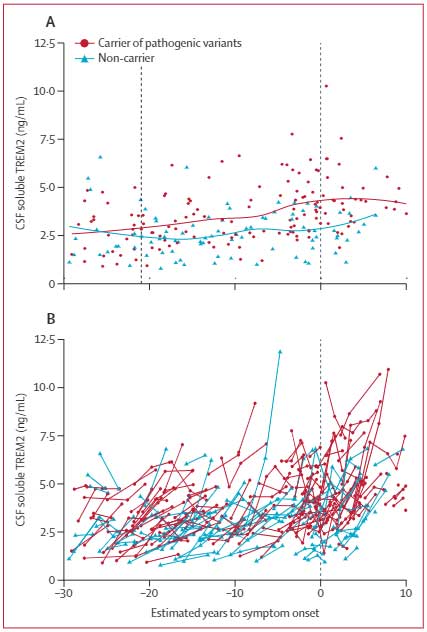
CSF中sTREM2の年間増加率はAβの年間増加率減少と相関がある
ベースラインのCSF中Aβ42およびAβ42/40比の低さとCSF中sTREM2の年間増加率上昇に有意な相関がありました。
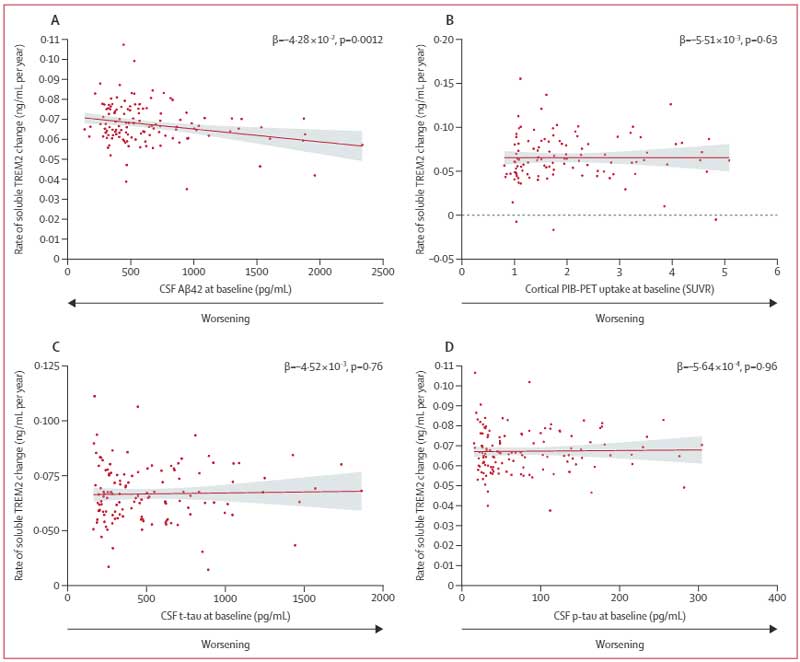
またCSF中sTREM2の年間増加率は、
- 発症前キャリア:CSF中Aβ42の年間減少率
- 発症キャリア:PiB-PETの変換増加率の減少
とそれぞれ相関を認めました。
ただし、ベースラインのPiB-PET、t-tau、p-tauなどとの相関はありませんでした。
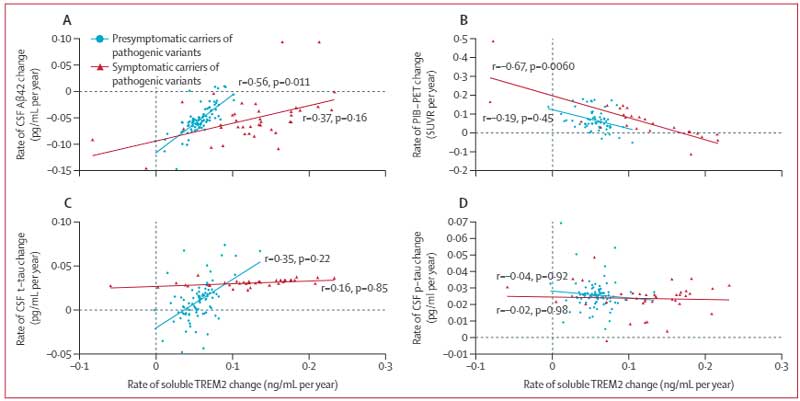
CSF中sTREM2の年間増加率はPiB-PETとCSF中p-tauの関係にも影響している
CSF中t-tauとp-tauとsTREM2の年間増加率etc.には有意な相関がありませんでしたが、
グループをsTREM2年間増加率の中央値で2群に分けると、
CSF中sTREM2の年間増加率が中央値より高い群では、PiB-PETの年間増加率が高いほどCSF中p-tauの年間増加率の高いのに対し、
CSF中sTREM2の年間増加率が中央値より低い群ではその相関が逆になる、という結果が得られ、
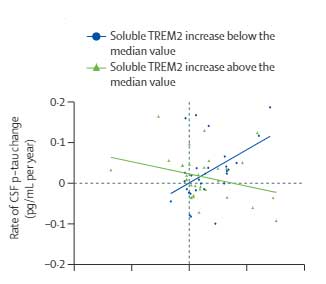
sTREM2がAβ沈着とタウ病理の関係に影響を及ぼしている可能性が示唆されました。
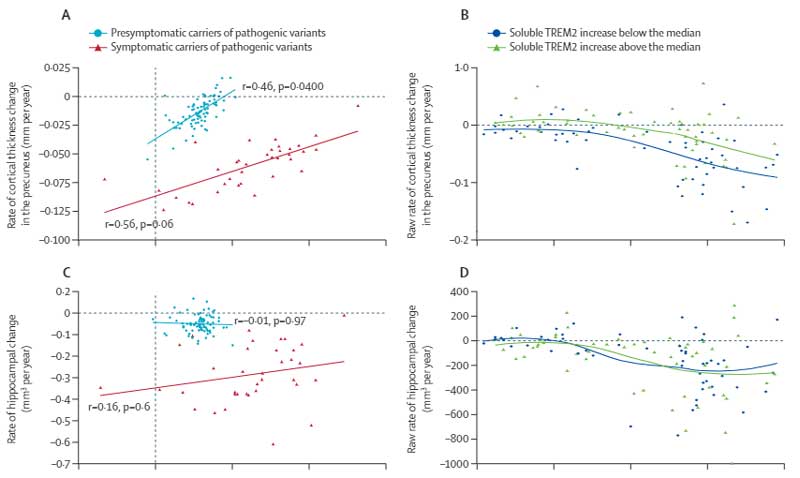
CSF中sTREM2の年間増加率は脳皮質の萎縮率と逆相関する
MRIで測定した皮質の厚さとCSF中sTREM2の年間増加率との関係を調べたところ、
発症前キャリア群では、CSF中sTREM2の年間増加率が高いと、皮質の萎縮率が低い傾向にある事がわかりました。
ただ、海馬の萎縮率とは相関がありませんでした。

CSF中sTREM2の年間増加率は認知機能低下と逆相関する
また、CSF中sTREM2の年間増加率と認知機能の年間低下率を調べたところ、
発症前キャリアの群では、CSF中sTREM2の年間増加率が高い程、認知機能低下がマイルドになっている事がわかりました。
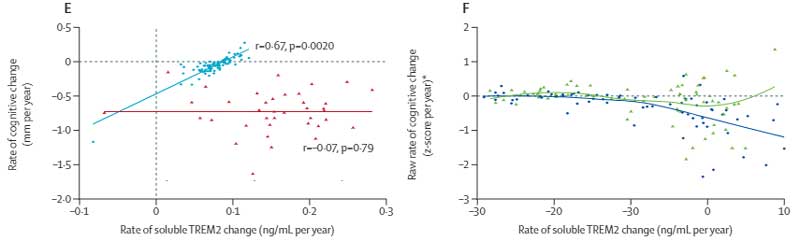
・
・
・
以上の結果から、
- アミロイドETでAβ沈着が確認される前でCSF中Aβ量に変化が起こる時期の、Aβシードの段階から、sTREM2は髄液中で増えている
- 認知症発症の21年くらい前からTREM2は活性化し、sTREM2が髄液中で増えている
- TREM2の活性化はAβ蓄積やその後のタウ病理、脳萎縮、認知機能低下等に保護的に働いている可能性がある
という事が示唆されました。
Our findings in autosomal dominant Alzheimer's disease position the TREM2 response within the amyloid cascade immediately after the first pathological changes in Aβ aggregation and further support the role of TREM2 on Aβ plaque deposition and compaction. Furthermore, these findings underpin a beneficial effect of TREM2 on Aβ deposition, Aβ-dependent tau pathology, cortical shrinkage, and cognitive decline. Soluble TREM2 could, therefore, be a key marker for clinical trial design and interpretation. Efforts to develop TREM2-boosting therapies are ongoing.
My View
髄液中の可溶性TREM2がADの早期バイオマーカーになるという事は注目されており、日本の久山研究でも「ADと血管性認知症の発症リスクを予測できる」という報告がありますが [12]、
今回はその髄液中sTREM2の年間増加率を他のバイオマーカーの年間増加率と比較することで、TREM2が脳内でAD病理と戦っている痕跡が浮かび上がってきたような印象を持ちました。
sTREM2の重要性を示唆する論文、という意味でも重要だとは思いますが、
「データの解析の仕方によって色々見えてくるものがある」
という事を教えてくれたようで、個人的に大変勉強になりました。
自分の今後の研究にも活かしていきたいです。
References
- Guerreiro R, Wojtas A, Bras J, Carrasquillo M, Rogaeva E, Majounie E, Cruchaga C, Sassi C, Kauwe JS, Younkin S, Hazrati L, Collinge J, Pocock J, Lashley T, Williams J, Lambert JC, Amouyel P, Goate A, Rademakers R, Morgan K, Powell J, St George-Hyslop P, Singleton A, Hardy J; Alzheimer Genetic Analysis Group. TREM2 variants in Alzheimer's disease. N Engl J Med. 2013 Jan 10;368(2):117-27. doi: 10.1056/NEJMoa1211851.Epub 2012 Nov 14. PMID: 23150934; PMCID: PMC3631573.
- Jonsson T, Stefansson H, Steinberg S, Jonsdottir I, Jonsson PV, Snaedal J, Bjornsson S, Huttenlocher J, Levey AI, Lah JJ, Rujescu D, Hampel H, Giegling I, Andreassen OA, Engedal K, Ulstein I, Djurovic S, Ibrahim-Verbaas C, Hofman A, Ikram MA, van Duijn CM, Thorsteinsdottir U, Kong A, Stefansson K. Variant of TREM2 associated with the risk of Alzheimer's disease. N Engl J Med. 2013 Jan 10;368(2):107-16. doi: 10.1056/NEJMoa1211103.Epub 2012 Nov 14. PMID: 23150908; PMCID: PMC3677583.
- Jay TR, Miller CM, Cheng PJ, Graham LC, Bemiller S, Broihier ML, Xu G, Margevicius D, Karlo JC, Sousa GL, Cotleur AC, Butovsky O, Bekris L, Staugaitis SM, Leverenz JB, Pimplikar SW, Landreth GE, Howell GR, Ransohoff RM, Lamb BT. TREM2 deficiency eliminates TREM2+ inflammatory macrophages and ameliorates pathology in Alzheimer's disease mouse models. J Exp Med. 2015 Mar 9;212(3):287-95. doi: 10.1084/jem.20142322.Epub 2015 Mar 2. PMID: 25732305; PMCID: PMC4354365.
- Wang Y, Cella M, Mallinson K, Ulrich JD, Young KL, Robinette ML, Gilfillan S, Krishnan GM, Sudhakar S, Zinselmeyer BH, Holtzman DM, Cirrito JR, Colonna M. TREM2 lipid sensing sustains the microglial response in an Alzheimer's disease model. Cell. 2015 Mar 12;160(6):1061-71. doi: 10.1016/j.cell.2015.01.049.Epub 2015 Feb 26. PMID: 25728668; PMCID: PMC4477963.
- Leyns CEG, Gratuze M, Narasimhan S, Jain N, Koscal LJ, Jiang H, Manis M, Colonna M, Lee VMY, Ulrich JD, Holtzman DM. TREM2 function impedes tau seeding in neuritic plaques. Nat Neurosci. 2019 Aug;22(8):1217-1222. doi:10.1038/s41593-019-0433-0.Epub 2019 Jun 24. PMID: 31235932; PMCID: PMC6660358.
- Yuan P, Condello C, Keene CD, Wang Y, Bird TD, Paul SM, Luo W, Colonna M, Baddeley D, Grutzendler J. TREM2 Haplodeficiency in Mice and Humans Impairs the Microglia Barrier Function Leading to Decreased Amyloid Compaction and Severe Axonal Dystrophy. Neuron. 2016 Oct 5;92(1):252-264. doi:10.1016/j.neuron.2016.09.016. PMID: 27710785.
- Schlepckow K, Kleinberger G, Fukumori A, Feederle R, Lichtenthaler SF, Steiner H, Haass C. An Alzheimer-associated TREM2 variant occurs at the ADAM cleavage site and affects shedding and phagocytic function. EMBO Mol Med. 2017 Oct;9(10):1356-1365. doi: 10.15252/emmm.201707672. PMID: 28855300; PMCID: PMC5623859.
- Kleinberger G, Yamanishi Y, Suárez-Calvet M, Czirr E, Lohmann E, Cuyvers E, Struyfs H, Pettkus N, Wenninger-Weinzierl A, Mazaheri F, Tahirovic S, Lleó A, Alcolea D, Fortea J, Willem M, Lammich S, Molinuevo JL, Sánchez-Valle R, Antonell A, Ramirez A, Heneka MT, Sleegers K, van der Zee J, Martin JJ, Engelborghs S, Demirtas-Tatlidede A, Zetterberg H, Van Broeckhoven C, Gurvit H, Wyss-Coray T, Hardy J, Colonna M, Haass C. TREM2 mutations implicated in neurodegeneration impair cell surface transport and phagocytosis. Sci Transl Med. 2014 Jul 2;6(243):243ra86. doi: 10.1126/scitranslmed.3009093. PMID: 24990881.
- Suárez-Calvet M, Araque Caballero MÁ, Kleinberger G, Bateman RJ, Fagan AM, Morris JC, Levin J, Danek A, Ewers M, Haass C; Dominantly Inherited Alzheimer Network. Early changes in CSF sTREM2 in dominantly inherited Alzheimer's disease occur after amyloid deposition and neuronal injury. Sci Transl Med. 2016 Dec 14;8(369):369ra178. doi: 10.1126/scitranslmed.aag1767. PMID: 27974666; PMCID: PMC5385711.
- Suárez-Calvet M, Kleinberger G, Araque Caballero MÁ, Brendel M, Rominger A, Alcolea D, Fortea J, Lleó A, Blesa R, Gispert JD, Sánchez-Valle R, Antonell A, Rami L, Molinuevo JL, Brosseron F, Traschütz A, Heneka MT, Struyfs H, Engelborghs S, Sleegers K, Van Broeckhoven C, Zetterberg H, Nellgård B, Blennow K, Crispin A, Ewers M, Haass C. sTREM2 cerebrospinal fluid levels are a potential biomarker for microglia activity in early-stage Alzheimer's disease and associate with neuronal injury markers. EMBO Mol Med. 2016 May 2;8(5):466-76. doi: 10.15252/emmm.201506123. PMID: 26941262; PMCID: PMC5120370.
- Piccio L, Deming Y, Del-Águila JL, Ghezzi L, Holtzman DM, Fagan AM, Fenoglio C, Galimberti D, Borroni B, Cruchaga C. Cerebrospinal fluid soluble TREM2 is higher in Alzheimer disease and associated with mutation status. Acta Neuropathol. PMCID: PMC4867123.
- Ohara T, Hata J, Tanaka M, Honda T, Yamakage H, Yoshida D, Inoue T, Hirakawa Y, Kusakabe T, Shibata M, Teraoka T, Kitazono T, Kanba S, Satoh-Asahara N, Ninomiya T. Serum Soluble Triggering Receptor Expressed on Myeloid Cells 2 as a Biomarker for Incident Dementia: The Hisayama Study. Ann Neurol. 2019 Jan;85(1):47-58. doi: 10.1002/ana.25385. Epub 2018 Dec 28. PMID: 30485483.
- Morenas-Rodríguez E, Li Y, Nuscher B, Franzmeier N, Xiong C, Suárez-Calvet M, Fagan AM, Schultz S, Gordon BA, Benzinger TLS, Hassenstab J, McDade E, Feederle R, Karch CM, Schlepckow K, Morris JC, Kleinberger G, Nellgard B, Vöglein J, Blennow K, Zetterberg H, Ewers M, Jucker M, Levin J, Bateman RJ, Haass C; Dominantly Inherited Alzheimer Network. Soluble TREM2 in CSF and its association with other biomarkers and cognition in autosomal-dominant Alzheimer's disease: a longitudinal observational study. Lancet Neurol. 2022 Apr;21(4):329-341. doi: 10.1016/S1474-4422(22)00027-8. PMID: 35305339; PMCID: PMC8926925.