高齢者の体内では、「炎症」関連のマーカーが高くなっており、脳内では健常人でも軽度の炎症が起こっています。
私は野生型マウス (C57BL/6J) 脳内を若齢と老齢で比較した事があるのですが、
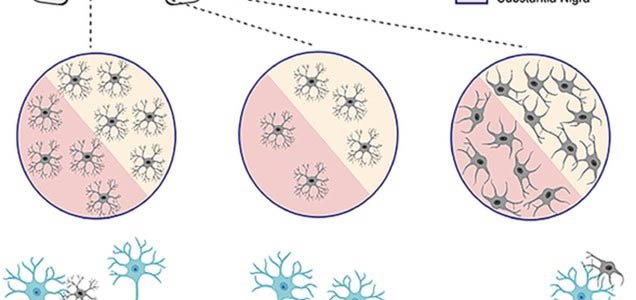
老齢マウスの脳内では、アストロサイトおよびミクログリアの増生が顕著で、初めて見た時に
「健康なのに、年をとったというだけでこんなに脳内環境が違うのか。」
と、大変驚いたのを覚えています。
この「炎症」は、認知機能低下、神経変性、アテローム性動脈硬化症などの数多くの加齢関連疾患の原因の1つと考えられています [1, 2, 3]。
しかしながら、この 「加齢と炎症」についての詳細なメカニズムについてはまだまだわからない事が多いです。
今回、アメリカ・スタンフォード大学の Dr. Andreasson らの研究グループは、加齢によりマクロファージの代謝が滞り、それを改善すると認知機能低下も改善する、という研究結果を報告しました [4]。
マクロファージの代謝を促進すると、加齢による認知機能低下が改善する
免疫細胞のホメオスタシスが加齢と密接に関係しており、特に、加齢したマクロファージが免疫低下を引き起こすことはこれまで報告されていた [5]。
著者らはさらに、炎症の中枢であるプロスタグランジE2 (prostaglandin E2, PGE2) に注目した。
65歳以上の高齢者の血液から単離したマクロファージでは、35歳以下の若者の血液から単離したマクロファージと比べて、PGE2の産生量が上昇していた。
さらに、PGE2 を培養マクロファージに処置すると、細胞の解糖系が落ち、ミトコンドリアの酸素消費量が用量依存的に低下した。
PGE2は、4種類のレセプターのうち、EP2 レセプターに特異的に結合し、骨髄系の代謝やエネルギー代謝に関与していた。
次に著者らは、PGE2 → EP2 → エネルギー代謝の低下 のメカニズムについてマウスを使って検証した。
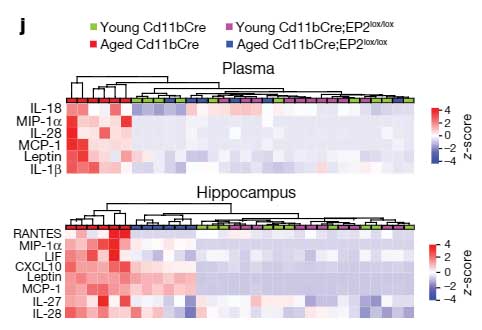
老齢マウス (20mo) では、血漿および脳内の PGE2 レベルおよび EP2 が上昇していた。
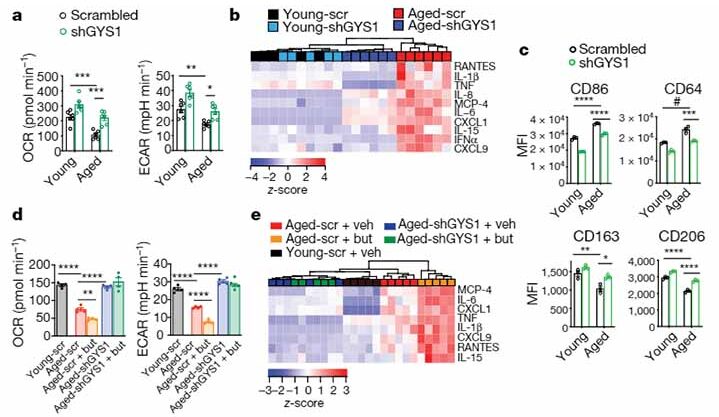
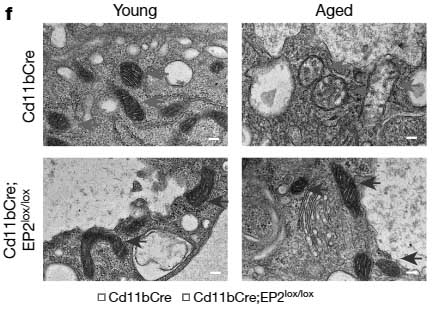
Cre-loxP システムで骨髄系細胞特異的に EP2 を半分程度に抑える (Cd11bCre;EP2 lox/lox) と、老齢でもミトコンドリアの代謝や解糖系レベルが若齢と同程度まで保たれ、サイトカインのプロファイルも若齢マウスとほぼ同じだった。
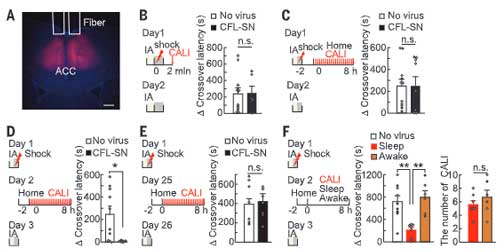
野生型の老齢マウスでは、シナプス後電位の長期増強が低下し、認知機能が落ちていたが、Cd11bCre;EP2 lox/lox の老齢マウスではどちらとも保たれていた。
さらに、EP2 シグナルを抑える薬剤 (C52) を老齢マウスに1ヶ月間投与すると、炎症性サイトカインの状態が若齢と同程度にまで保たれ、ミクログリアの活性も抑えられていた。
C52は、解糖系およびミトコンドリアのエネルギー代謝も改善させ、加齢に伴う認知機能低下も改善した。
以上の結果は、加齢による認知機能低下が、不可逆的なものではなく、EP2 シグナルを抑える薬剤の投与により、回復可能であることを示唆している。
References
- Franceschi C, Capri M, Monti D, Giunta S, Olivieri F, Sevini F, Panourgia MP, Invidia L, Celani L, Scurti M, Cevenini E, Castellani GC, Salvioli S. Inflammaging and anti-inflammaging: a systemic perspective on aging and longevity emerged from studies in humans. Mech Ageing Dev. 2007 Jan;128(1):92-105. doi: 10.1016/j.mad.2006.11.016. Epub 2006 Nov 20. PMID: 17116321.
- Nikolich-Žugich J. The twilight of immunity: emerging concepts in aging of the immune system. Nat Immunol. 2018 Jan;19(1):10-19. doi: 10.1038/s41590-017-0006-x. Epub 2017 Dec 14. Erratum in: Nat Immunol. 2018 Oct;19(10):1146. PMID: 29242543.
- Ferrucci L, Fabbri E. Inflammageing: chronic inflammation in ageing, cardiovascular disease, and frailty. Nat Rev Cardiol. 2018 Sep;15(9):505-522. doi: 10.1038/s41569-018-0064-2. PMID: 30065258; PMCID: PMC6146930.
- Minhas PS, Latif-Hernandez A, McReynolds MR, Durairaj AS, Wang Q, Rubin A, Joshi AU, He JQ, Gauba E, Liu L, Wang C, Linde M, Sugiura Y, Moon PK, Majeti R, Suematsu M, Mochly-Rosen D, Weissman IL, Longo FM, Rabinowitz JD, Andreasson KI. Restoring metabolism of myeloid cells reverses cognitive decline in ageing. Nature. 2021 Jan 20. doi: 10.1038/s41586-020-03160-0. Epub ahead of print. PMID: 33473210.
- Minhas PS, Liu L, Moon PK, Joshi AU, Dove C, Mhatre S, Contrepois K, Wang Q, Lee BA, Coronado M, Bernstein D, Snyder MP, Migaud M, Majeti R, Mochly-Rosen D, Rabinowitz JD, Andreasson KI. Macrophage de novo NAD+ synthesis specifies immune function in aging and inflammation. Nat Immunol. 2019 Jan;20(1):50-63. doi: 10.1038/s41590-018-0255-3. Epub 2018 Nov 26. PMID: 30478397; PMCID: PMC6768398.